Производство стали — это сложный физико-химический процесс, при котором протекают химические реакции в жидком металле и шлаке, а также на границах между жидким металлом шлаком, между шлаком и газовой печной средой.
Приготовление стали любым способом сопровождается химическими реакциями восстановления, окисления и соединения отдельных элементов и образующихся веществ между собой. Углеродистая сталь по своему химическому составу отличается он чугуна тем, что в ее составе содержание С, Si, Мn, Р и S находится в меньшем количестве, чем в чугуне. Легированные стали в отдельных случаях содержат повышенное количество отдельных легирующих элементов. Поэтому при производстве стали некоторые элементы из металла удаляются, а другие вводятся в расплавленный металл.
При рассмотрении химических реакций учитывается, что некоторые из них являются экзотермическими, а другие — эндотермическими. Элементы, участвующие в экзотермических реакциях, энергичней вступают во взаимодействие, когда металл имеет более низкую температуру и, наоборот, в перегретом металле более энергично протекают реакции тех элементов, которые взаимодействуют с поглощением тепла.
При плавке чугуна или стали в первую очередь окисляется железо (согласно закону действующих масс), ввиду превалирующего его содержания в сплаве:
2Fe+O2→2FeO,
4FeO+
O2→2Fe2O3,
Однако ввиду того, что ряд примесей, содержащихся в металле, имеют большее сродство к кислороду, чем железо, они восстанавливают железо из окислов. Поэтому окисление примесей производится как непосредственно кислородом, так и за счет реакций с окислами железа Последовательность реакций подчиняется законам химического сродства:
Si + O2 →Si O2, Si + 2FeO→2Fe
+ SiO2,
2 Мn→O2 →2 МnО, Мn+FeO→Fe+МnО,
2С + O2→2СО, С + FeO→Fe+СО,
С +
O2→CO2,
4Р +
5O2→2Р2O5, 2P + 5FeO→5Fe +
P2O5
Удаление фосфора успешно протекает в металлургических чах с основной футеровкой Общий ход реакций, связанных с алением фосфора, будет следующим:
2 Р + 5 FeO→Р2О5+5Fe + 47 850 кал,
Р2О5 + 3 FeO→(FeO)3 Р2О5 + 52
360 кал,
(FeO)3 Р2О5 + 4СаО→(СаО)4
Р2О5 + 3 FeO + 108 340 кал.
Фосфор удаляют в начальный период плавки, создавая окислительные шлаки высокой основности Серу удаляют в металлургических печах с основной футеровкой при высокой основности шлака:
FeS+СаО↔CaS 4- FeO,
MnS+СаО↔CaS+МnО.
Эти реакции носят обратимый характер, и при наличии в шлаке повышенного количества FeO они идут в обратном направлении. Весьма благоприятные условия для удаления серы можно создать при плавке стали в электрических печах под восстановительным и карбидным шлаком:
FeS +СаО + С→CaS+Fe + СО,
MnS+СаО +С→CaS + Мn+СО,
3
FeS+СаС2 + 2 СаО→3 Fe+3CaS + 2 СО,
3MnS+CaC2+2CaO→3Мn+3CaS + 2СО.
Поэтому удаление серы протекает весьма успешно в электропечах, в которых легко создать восстановительную атмосферу.Закись железа растворяется в металле и шлаке. Закись железа в твердом металле является вредной примесью. Поэтому ее Стремятся удалить из металла во время плавки путем раскисления.
Шлак и металл можно рассматривать как две несмешивающиеся жидкости, находящиеся в равновесии, в которых растворяются FeO, FeS и другие соединения. По закону распределения отношение концентраций растворенных в этих жидкостях веществ есть величина постоянная при данной температуре, например:
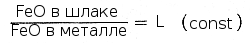
Отношение L называют коэффициентом распределения. В соответствии с этим законом процессы раскисления стали можно проводить в двух направлениях: в жидком металле путем осадочного раскисления, или в жидком шлаке путем диффузионного раскисления. При осадочном раскислении в жидкую сталь в конце плавки добавляют раскислители: ферромарганец, ферросилиций, алюминии и другие элементы, сродство к кислороду у которых больше, чем у железа:
FeO + Мn→Fe + МnО,
2FeO + Si→2Fe + SiO2,
3 FeO
+2 Al→3 Fe + Al2O3
При добавке раскислителей в металл они после раскисления частично остаются в металле в качестве примесей. Продукты раскисления также частично остаются, загрязняют металл неметаллическими включениями. Диффузионное раскисление стали ведется при помощи раскислителей, которые добавляются в шлак в виде порошков углеродистых веществ, молотого ферросилиция, порошка алюминия и т. п. Это приводит к понижению концентрации закиси железа в шлаке, а следовательно, и в металле, согласна рассмотренному выше закону распределения. В этом случае металл не загрязняется неметаллическими включениями. Для определения раскисленности стали в конце плавки берут технологические пробы.